2026.03.23
現在 人工知能(AI)を用いたマンモグラフィの読影が、進歩し、場合によっては人間の読影を凌駕する成績が出るようになってきています。少なくとも、人間の負担を減らし、発見率を上げることはすでに証明済みといってよく、確実な事実です。恐ろしいのはいったんAIの助けを借りるようになれば、人間の読影技術はそれによって進歩するのではなく、ほぼ確実に劣化することも指摘され始めています。いったん依存してしまえばもはや抜け出せないのです。
その問題はいつか触れるとして、最近、AIの助けを借りれば、定期的なマンモグラフィー検査で心血管疾患のリスクが高い女性を特定できる可能性があることが、ある後ろ向きコホート研究で示唆されました。
マンモグラフィの画像診断で、AIによって算出された乳房動脈石灰化の量が多いほど、内部検証コホートと外部検証コホートの両方で、その後の大きな心血管イベント(例えば狭心症、心筋梗塞など)のリスク増加と関連していました。例えば、高齢でリスクの高い外部検証コホートでは、乳房動脈石灰化が進行した女性は、追跡期間の中央値7年間で心血管イベントを経験するリスクが高くなっていました。
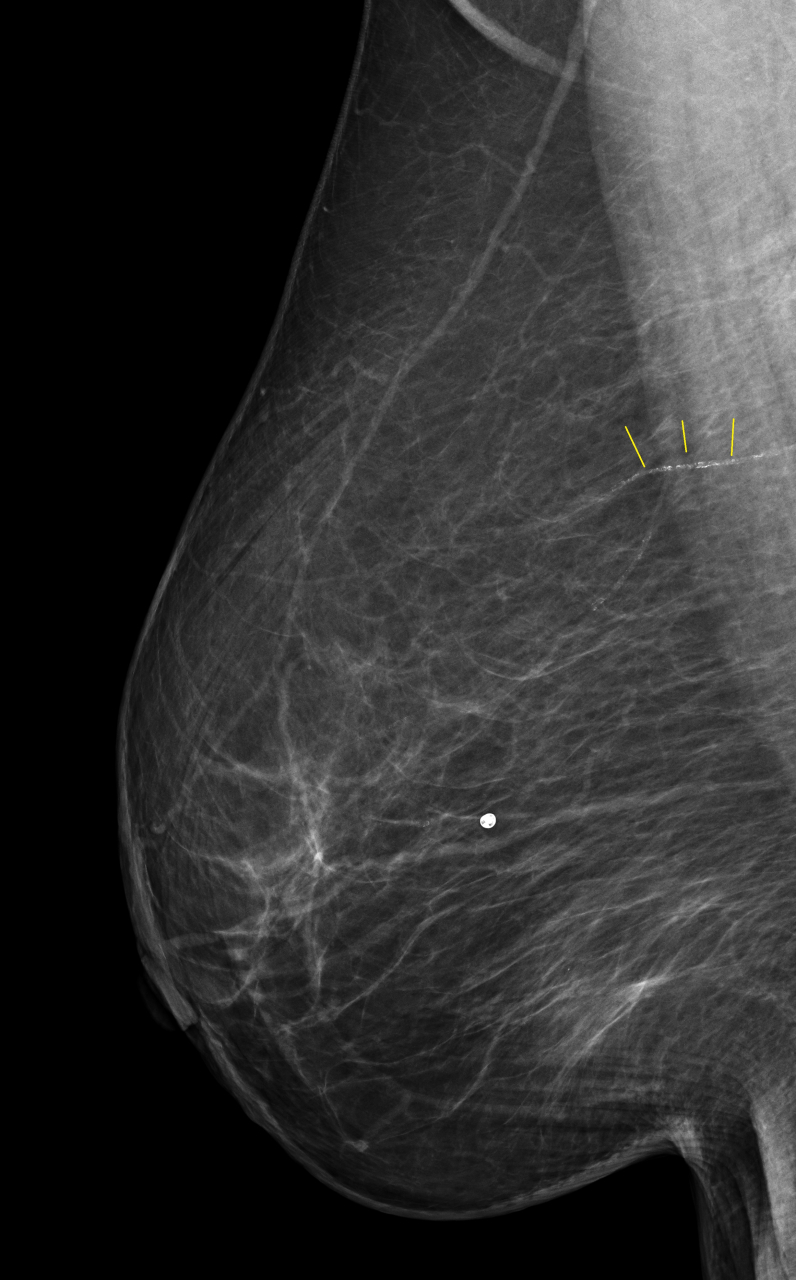
上記のMMGにおいて 黄色い線で示しているところは乳腺の動脈です。そこに沿って白い小さな点がびっしりと認められます。この動脈に”動脈硬化”が発生し、そこに石灰(カルシウム)が沈着することで描出されるようになったものです。
軽度の乳房動脈石灰化(>0-10 mm 2):調整済みハザード比 1.28(95%信頼区間 1.17-1.39)
*乳房動脈石灰化のない方と比べて心血管イベントを起こす可能性が1.28倍あるということ
中等度の乳房動脈石灰化(10~25 mm2 ):調整済みハザード比 1.79(95%信頼区間 1.55~2.06)
重度の乳房動脈石灰化(>25 mm2 ):調整済みハザード比 2.80(95%信頼区間 2.36-3.32)
「私たちの研究は、定期で行われるマンモグラフィー検査における、AIによる自動的な乳房内の動脈の石灰化の定量化が、大規模な多民族集団における心血管系有害事象の強力かつ独立した予測因子であることを示しています」と、アトランタのエモリー大学のハリ・トリヴェディ医師らは、この研究で示しました。
「この手法は、追加の放射線被曝なしに、定期的なマンモグラフィー検査中に心血管リスク評価を提供し、女性に対するより早期かつ効果的な予防医療を導く可能性がある」と彼らは結論付けました。
トリヴェディ氏らは、乳房内の動脈の石灰化が1mm²増加するごとに、主要な心血管イベントのリスクが2~3%有意に増加することを報告しました。この結果は、50歳未満の女性を含むすべての年齢層で有意であり、従来の危険因子やPREVENTリスクスコアとは無関係で、独立したものでした。(PREVENTリスクスコアは最近米国の学会において、汎用的な心血管リスク層別化ツールとして宣伝されたものです。)
「乳房内の動脈の石灰化の定量化は、PREVENTのような包括的なリスクモデルに取って代わることを意図したものではないことに留意することが重要です」と著者らは説明しています。「むしろ、乳房内の動脈の石灰化は、見過ごされがちなリスクの高い患者を特定し、かかりつけ医による正式な心血管リスク評価を促すための強力な指標として機能する可能性があります。」
「あなたがすでにマンモグラフィー検査を受けている女性の場合、この検査は、心臓の健康状態に関する重要な情報を提供し、コレステロール検査や投薬などの予防策について医師と話し合うきっかけにもなります」と、トリヴェディ氏はプレスリリースで述べています。「臨床医にとっては、現在見過ごされている心血管疾患リスクの高い女性を特定するための実用的な方法となります。」
マンモグラフィ検査は定期的に行われるものであるため、それと一緒に心血管リスクも評価するスクリーニングが可能であるならば、それには大きな意味があります。なぜなら、心血管疾患(CVD)は米国では重要な死亡原因の一つだからです。
米国では、女性における乳がんは一貫して診断は遅れがちで、かつ受けられる治療も十分とは言えない状態にあります。乳がんの早期発見のためのマンモグラフィーの受検率は40歳以上の女性において70%近くに達しています。
実際には、マンモグラフィーで乳房内の動脈の石灰化が指摘された場合、心血管疾患リスク因子の最適化と心不全予防を並行して行うべきであると、カリフォルニア大学サンディエゴ校のロリ・ダニエルズ医師は付随する論説で提言しています。
「重要なのは、乳房内の動脈の石灰化は、単純に心臓の冠動脈石灰化とイコールではなく、代用指標ではないということです」と彼女は書いている。「両者は相関関係にあるものの、病理学的には異なります。しかし動脈中膜に主に存在している乳房内の動脈の石灰化は、血管の老化と動脈硬化を反映しています。この区別は臨床的に重要です。なぜなら、これらの併存疾患は心室硬化、ひいては心不全、特に駆出率が保たれた心不全の発症と強く関連しているからです」と彼女は付け加えました。
トリヴェディ氏らは、この後ろ向き研究において、スクリーニングマンモグラフィーを受けた2つの医療システムに属する女性を対象としました。1つはエモリー・ヘルスケアの内部(自施設)検証コホート(n=74,124、平均年齢55.5歳)、もう1つはメイヨー・クリニックの外部(他施設)検証コホート(n=49,638、平均年齢59.5歳)です。主要心血管イベントおよびPREVENTのリスク変数は、電子カルテから抽出されました。主要心血管イベントには、急性心筋梗塞、脳卒中、心不全、および全死因死亡が含まれます。
乳房内の動脈の石灰化分析では左右両方の乳房を対象としましたが、各患者の最終結果としては、検出された値が最も高かった側の乳房のみを使用しました。最終的に、研究参加者の16.1%(内部コホート)および20.6%(外部コホート)で乳房内の動脈の石灰化が検出されました。
「本研究は、単一の包括的なリスクモデルをある施設で開発し、それを別の施設で外部検証するという従来の方法とは異なり、異なる集団における乳房内の動脈の石灰化の定量化の予後予測価値を検証することを目的として設計されました」と著者らは述べています。「言い換えれば、私たちの目標は、集団全体に適用できる『最適な』リスクモデルを作成することではなく、ベースラインリスクが異なる集団においても、独立した予測因子としての乳房内の動脈の石灰化の付加的な価値を示すことでした。普遍的なリスクモデルを開発することの難しさは、動脈硬化性心血管疾患やPREVENTリスク計算ツールが特定の集団にはうまく適用できないことを示すデータにも表れている」と彼らは付け加えました。
(この部分は難しいですが、こうした検証はある程度施設に依存していて、ある施設では成り立つけれども、他施設では成り立たない、がありうるということをできるだけ排除するように考えた研究です、と言っています。つまりどの施設であっても、このことは成り立つ、と言っているわけです。)
特筆すべき点として、この研究は人種的にかなり多様であったものの、アジア系、ヒスパニック系、ネイティブアメリカンの代表性は依然として限られていた。
「この研究のユニークなことは、実用的で直感的な報告指標である乳房内の動脈の石灰化を面積(mm²)として定量化した点にあります。あるなしの感覚的なものを、定量化し、それが心血管疾患のリスクにつながることが証明されました。これは単なる主観ではありません。物理的な単位を用いることで、ベンダー間の標準化を加速させ、再現可能な閾値を容易にし、実装ワークフローを円滑化できる可能性があります。(難しくいっていますが、つまりAIに組み込んでしまえば、どの施設でも心疾患リスクを同時に判定できるようになる可能性がある、」
「乳房内の動脈の石灰化の面積をわれわれは指標としましたが、最終的にどのような報告指標が採用されるかにかかわらず、女性の重要な死因である心疾患の予防を推進するために、女性が既に信頼を寄せている接点であるマンモグラフィ検診を活用し、乳房内の動脈の石灰化の評価を観察段階から実施段階へと移行させるべき時が来ています」と彼女は結論付けました。
2026.03.07
AI(アリミデックスやフェマーラ、アロマシン)なのか、SERM(タモキシフェン、トレミフェン)なのか、これが実はとても深い問題を含んでいるのです。
簡単に言い切れば、乳がんによる死亡を抑制してくれる効果はAIを100点としたらタモキシフェンは89点です。たしかに弱い。
そして副作用に関しては代表的なものを挙げるとタモキシフェンは子宮体癌、AIは骨粗しょう症になるでしょう。
え、副作用ががんなの、癌の再発を抑えるために他のガンが発生してたら意味ないじゃん。それならAIの圧勝でしょう。皆さんもそう思いますか?私は違う考え方をします。
これに関して、詳しくはこのブログで何度も触れてきましたが、子宮体がんはタモキシフェンを飲んでいなくても65歳以上であれば年間千人に一人は発症します。つまり0.1%です。飲んでいる方で多く見積もって1000人に二人なので0.2%と考えられます。
AIによる骨折の発生ですが、5年以上継続した場合、1.35倍になります。65歳以上の女性では10万人あたり年間約 646人 が大腿骨骨頭骨折を経験するとされていますので、千人に6人、0.6%とされます。もちろんこれは大腿骨骨頭に限定していますので、腰椎の圧迫骨折なども含めるともっと確率は上がります。
そしてもう一つ大事な情報ですが、タモキシフェンは骨を強くする、守る方向に働きます。AIが子宮体がんの確率を落とす効果があるかについては報告はありません。そしてタモキシフェンの子宮内膜への刺激は薬をやめればなくなります。つまり可逆的ですが、AIによって進んだ骨粗鬆症は、たとえAIをやめても原則元には戻せません。
現状 乳がん術後のホルモン治療は10年継続するように指導されている方は多いと思いますが、閉経後に限定した場合、その多くは60歳以上の女性になると思いますが、70歳になるまで10年ずっとAIで行くかどうかは、慎重でなければならない、と私は考えています。がんを抑制する効果は高くても、骨が脆くなってしまって、Quality of Life(=QOL) 生活の質、が下がってしまったら、元も子もない、と考えているからなのです。


ノースカロライナ大学チャペルヒル校ラインバーガー総合がんセンターのダニエル・R・リチャードソン医学博士(理学修士)らが最近発表した研究結果では、706人の進行したがん患者さんのうち、生存期間の延長を優先したのはわずか8.4%であったのに対し、QOLの維持を優先したのは71.7%で、残りはどちらでもないか中立だったと報告しました。
さらにクラスターランダム化試験の二次分析によると、進行がんを患う高齢患者は生存期間の延長よりも生活の質(QoL)の維持を優先する傾向があり、そして結局患者さんがどちらを希望し、優先しているかどうかに関わらず、こうした好みによって患者の転帰に差は生じなかったと言うこともわかりました。つまり事前の治療変更、またはグレード 3 ~ 5 の治療関連有害事象 (TRAE)、入院、死亡率などの下流の臨床結果がどちらを優先するかが異なる患者グループ間で比較しても結局差がなかったのです。それはおそらくそういった患者さんの志向によって、治療者が内容を変更することがないことも示していると考えられました。
編集者のメモオクラホマシティにあるオクラホマ大学ヘルス・スティーブンソンがんセンターの医学博士、公衆衛生学修士、経営学修士であり、JAMA Oncologyの副編集者でもあるライアン・D・ニップ氏は、「がん患者の大半は高齢者であり、この集団の QoL の優先事項を評価し、対処する研究をさらに進める必要がある」と書いています。「この研究が示したように、がんを患う高齢者は生存期間の延長よりもQOLの維持を優先することが多いのですが、私の知る限り、こうした患者のQOL向上を目的とした介入を評価した研究はほとんどありません」と彼は指摘しました。「こうした取り組みには、患者中心のケアを促進し、老年腫瘍学の分野で行われている革新的な研究に基づいた介入の開発と検証が含まれます。」

乳がん術後のホルモン治療に関しても、この研究と同じことが言えそうな気がします。
少なくとも65歳を超えた方に関しては、ホルモン治療を受けるかどうか、だけにとどまらず、その得られる効果、そして副作用も説明した上で、AIを選ぶか、SERMを選ぶか、話し合う必要があると私は考えます。そしてはそれはホルモン治療開始のその時だけではなく、たとえば1年ごとに副作用の出現やその程度を見極めながら、繰り返し話し合っていく必要があると思うのです。
そしてそうして患者さんの志向を聞いて、ホルモン剤を選んでいった場合と、医療側が最善と思われるホルモン剤を一方的に決めていった場合で、生存予後にどの程度の差が生じるのか、生じないのか? そしてその患者さんの人生の満足度にどのような影響が及ぶのか、ライアン先生の主張されているように、きちんと調査されるべきではないか、と私は考えます。
まとめ
進行がんを患う高齢者を対象とした研究では、生存期間の延長を優先したのはわずか8.4%であったのに対し、生活の質(QoL)の維持を優先したのは71.7%でした。
生存を優先した患者とQOLを優先した患者の間で、初期治療の変更や臨床結果に有意差はありませんでした。
これらのデータは、現在の腫瘍治療提供システムが患者の好みに対応できていないことを示唆していると研究者らは述べました。
私はこの結果をAIとSERMに準えて(なぞらえて)みました。
乳がんを患った高齢者を対象とした研究では、生存期間の延長を優先したのはXX%であったのに対し、生活の質(QoL)の維持を優先したのはZZ%でした。(もちろんまだそのデータはありません。)
生存を優先した患者とQOLを優先した患者の間で、初期治療の変更や臨床結果に有意差は〇〇した。(差が出るでしょうか? 出ないのでしょうか?)
このデータから、今後は特に高齢の女性乳がん患者さんにおいては、患者さんの志向を加味してホルモン剤を臨機応変に決定していく****(べきなのでしょうか? まだわかっていません。)
ご予約専用ダイヤル
079-283-6103