乳がん術後に放射線治療を行うことで、局所の再発を極端に抑制することができることはよく知られています。特に乳房を温存する切除を行った後では、がんがあった部位周辺の取り残しを根絶するために、そしてリンパ節転移があった症例では、がんからリンパ節、リンパ節からその周辺へのがんの流れを焼いておくことで、局所再発をしっかりと抑制できます。
しかしたとえば乳腺の端のほうにあった小さな乳がんであっても、温存切除で残された乳腺すべてに放射線治療をする必要はあるのでしょうか?
乳がんがしこりが十分小さく、またリンパ節転移もなく、さらに切除後の病理のプレパラートでみても、がんのしこりの周辺にがんが広がる傾向が認められない場合、腋窩や、鎖骨の周辺への放射線治療はいらないのではないでしょうか?
また手術の前に抗がん剤による治療を受け、その後の手術でがんがほぼ消失してしまったことが証明されたときに、術後の放射線治療は本当に必要なのでしょうか?
今年 バルセロナで開催された第15回欧州乳がん会議(EBCC15)で発表された、10年間にわたるオランダの研究(RAPCHEM; BOOG 2010-03)によって、化学療法と手術後に、患者個々のリスクに合わせて放射線療法を行ったとしても、乳がんの再発率は低いままであることがあきらかになりました。
この研究では、化学療法と手術後に患者のリンパ節に乳がん細胞の痕跡が見られるかどうかに応じて、オーダーメイドの放射線治療が選択されました。リンパ節にがんの痕跡が残っていない女性の場合には、本研究では放射線治療を最小限に抑えるか、あるいは全く行わないことを選択しました。治療規模を縮小することで、もちろん患者の副作用を軽減することができます。
この研究は、オランダのマーストリヒト放射線腫瘍研究所(Maastro)で放射線腫瘍医研修中のフルール・モーリッツ医師によって発表されました。彼女は次のように述べています。「乳がん患者の多くにとって、最初の治療は化学療法です。これにより、手術前に腫瘍を縮小させ、体内に広がり始めているがん細胞を死滅させることができます。いっぽう放射線療法は、特に乳房全体ではなく腫瘍のみを切除する手術を受けた患者や、リンパ節にがんの兆候が見られる患者において、乳がんの再発リスクを低減することが知られています。この研究では、手術前に化学療法を受けた際にがんが良好な反応を示した患者において、放射線療法を縮小できるかどうかを検証しました。」
本研究には、2011年から2015年の間にオランダの17の癌センターで治療を受けた848人の患者が含まれました。各患者は、5cm未満の小さな乳房腫瘍を持ち、様々な検査において1つ、2つ、または3つのリンパ節に転移があると診断されています。
術前に化学療法を施行し、その後に手術を行った後、患者さんは3つの異なるリスクグループに分類されました。
リンパ節にがんの転移がないと診断された患者さんは低リスクと分類され、手術で腫瘍が切除され、乳房は温存された場合は残った乳房への放射線療法が行われ、乳房全摘術を受けた場合は放射線療法は行われませんでした。(筆者注:現在の通常の治療では、化学治療後に転移の兆候が消えていても、腋窩や、鎖骨周囲に放射線治療を加えます
リンパ節に1~3個の転移の兆候が見られた患者は中リスクに分類され、近くのリンパ節には照射せずに乳房領域のみに放射線療法を行いました。(筆者注:現在の通常の治療では、化学治療後に転移の兆候が残っていたら、確実に腋窩や、鎖骨周囲にも放射線治療を加えます。)
4つ以上のリンパ節に転移の兆候が残っていた患者さんは高リスクと分類され、乳房領域および周囲のリンパ節への放射線療法による治療が行われました。
その後の10年間で、追跡調査を完了した838人の患者のうち24人(2.9%)が、乳房、胸壁、またはリンパ節に再発したが、体内の他の部位への癌の転移は認められませんでした。低リスク群では291人中7人(2.4%)が再発し、中リスク群では370人中12人(3.2%)が再発し、高リスク群では177人中5人(2.8%)が再発しました。(筆者注:つまり差がありませんでした。)
マウリッツ博士は、「私たちの研究結果は、リンパ節の癌治療における化学療法の効果に応じて、副作用を抑えるために放射線療法の範囲を調整したとしても、乳房とその周辺領域における再発率が非常に低く、安心できる結果につながることを示しています。特定の患者グループでは、放射線療法を全く行わなくても、再発率が非常に低いことが確認されています」と述べました。
彼女は続けて、「本研究の大きな強みは、この患者群に対する放射線療法の個別化による効果を10年間にわたって初めて実証した点です。逆に本研究の限界というか、問題点は、研究対象となった患者のほとんどが腋窩リンパ節郭清術を受けたことです。この手術は10年前には一般的でしたが、現在の臨床現場ではあまり行われていません。(筆者注:腋窩郭清を全くせずに、つまりセンチネルリンパ節生検だけであったなら、同じ結果が出るかわからない、ということです。)また本研究では、放射線療法を受けた患者と受けていない患者を比較していません。(筆者注:本研究では全く行わなくても大丈夫かまでは検討していません。)
最終的な結論を得るには、米国/NSABP(ClinicalTrials.gov識別子NCT01872975)による無作為化試験の結果を待つ必要があります。結果は3年後に発表される予定です。」と述べました。

私がこの発表にひかれたのは、放射線治療をオーダーメイドする、という観点です。
いまはいい意味でも悪い意味でも、”ガイドライン”がガチガチに整備されていて、いわゆる主治医の判断が入り込む余地はなくなっています。これによって全国どこに行っても同じレベルの治療が受けられるようになりましたが、逆に患者さんと主治医が話し合って治療を決定していく、という要素がほぼなくなってしまっています。極端に言えば、AIに治療を決めてもらっても、主治医に決めてもらっても、変わりがないのです。誰がやっても一緒、いやむしろAIのほうが最新のガイドラインまですべて網羅しているので、優れている可能性があります。
ただ治療を受けるのは患者さんであり、人間であり、個別に訴えを持ち、治療に対する希望があります。
このブログでもたびたび述べていますが、たとえば閉経後乳がんじゅつごのホルモン治療は現在ほぼアロマターゼ阻害剤(AI)一択です。SERM(タモキシフェン)より明らかにがんの再発も、乳がんによる死亡も抑制することが分かっています。
でもAIは骨粗しょう症を引き起こします。関節痛、膝の痛みや、指のこわばり、腰痛などの原因になります。そして長期投与で骨がもろくなってしまうのです。
これは私自身の希望ですが、私は長生きはしたいですが、寝たきりになるくらいなら、早くいきたい、子供に迷惑をかけて長生きするのは嫌です。だから骨粗鬆が明らかになるまではAIでもいいですが、それが分かれば早急にむしろ骨を守ってくれるタモキシフェンに変更してほしい。
でもいまのところガイドラインには骨塩定量、つまり骨粗しょう症の検査結果に応じて、SERMとAIを使い分ける提案はされていません。
放射線治療も同様です。
私はNSMやSSM、つまり皮膚を温存して乳房は全摘し、インプラントで同時再建する術式をDirect to Implantと呼ぶのですが、この手術は温存切除であり、全的ではない、だから放射線治療を加えたほうがいい、と考えています。
しかし現状 ガイドラインでは放射線治療はいらないとされています。
ただ再建された乳房全体に放射線治療を当てると、再建が失敗することを最大として様々な合併症を引き起こします。ですので、たとえばがんがあった部位の周辺だけは放射線治療をしておく、であるとか、血流が少ないため合併症の原因になりやすい、乳腺のTop、乳頭付近だけは避けて周辺だけは当てておく、乳頭より内側にがんがあった場合には、胸骨周囲には当てておく、など、個別に応じて放射線治療ができればいいのに、と考えていた時期がありました。
リスクがコントロールできれば、NSM、SSMの対象とできる疾患も広がります。
この研究のように、医師の裁量部分を増やす動きは、いままでの反動として重要なのではないか、と考えています。ガイドライン一辺倒で、思考停止となるのではなく、患者さんという人間が、医師という人間と話し合いながら治療を模索していく、そういう時代に戻ってほしい、とそう願っているのかもしれません。
2026.04.06
「先生、サプリメントとか、飲んじゃだめですか?」
これは患者さんから本当によく尋ねられる質問で、昔からずっと変わりません。
がんの治療には、手術・抗がん剤・放射線治療などの「標準治療」があります。
これに対して、「補完代替医療(ほかんだいたいいりょう)」とは、簡単に言い切ってしまうならばこれらの治療以外の方法を指します。補完医療と代替医療があるのですが、その違いは、補完医療は標準治療と「一緒に使う」もので、ヨガ、アロマ、サプリメントなどです。代替医療は標準治療の代わりに使うもので、民間療法のみで治療しようとする場合です。重要なのは、代替医療だけでがんを治すことは、現在の医学では証明されていないという点です。というよりも証明されればそれは標準治療だからです。
最近 JAMAという雑誌に、この質問に対するしっかりした答えが掲載されています。これをここでまとめてみたいと思います。

はじめに
過去数十年にわたる乳がんの外科的および内科的治療における革新により、乳がんの全生存率は向上しています。手術、化学療法、放射線療法、内分泌療法、免疫療法などの従来の治療法は確実に進歩し、結果を出しているにもかかわらず、一部の患者さんは依然として補完代替医療(CAM)を選択し、施行しています。そこで本研究では 乳がん患者におけるCAMと生存率との関連性を明らかにしたいと考えました。
方法ですが、本研究では、2011年から2021年にかけて乳がんと診断された女性患者に関する国立がんデータベースのデータを分析しました。生存期間は、従来治療群、従来治療と代替医療併用群、および無治療群の間で比較されました。データは2025年5月から2025年12月にかけて分析されました。補完療法または代替療法については、非医療従事者によって実施される治療と定義しました。
その結果について、乳がんの女性患者2,169,202人のうち、2,157,219人(年齢中央値[IQR]、62歳[52-71歳])がサンプルに含まれました。
合計2,106,665人(97.6%)が従来療法を受け、273人(<0.1%)がCAMのみを受け、568人(<0.1%)がCAMと従来療法の併用を受け、49,713人(2.3%)が治療を受けていませんでした。
従来療法を受けた患者と比較して、CAMのみを受けた患者(調整ハザード比[AHR]、3.67、95%信頼区間、3.03-4.44、P < .001)または治療を受けなかった患者(AHR、3.53、95%信頼区間、3.48-3.58、P < .001)は死亡リスクが最も高いという結果になりました。
*ハザード比ですが、「従来療法を受けた患者と比較して、CAMのみを受けた患者ではハザード比が3.67でした」という表現によって、従来療法を受けた患者と比較して、CAMのみを受けた患者では3.67倍死亡する確率が高い、という意味になります(筆者注)
従来療法とCAMを併用した患者は、従来療法のみを受けた患者と比較して、内分泌療法(ステージIIでは40.7%対65.2%、P < .001)および放射線療法(ステージIIでは59.5%対36.6%、P < .001)を受ける可能性が低いということが分かりました。
従来療法とCAMを併用した治療を受けた患者は、従来療法のみを受けた患者と比較して、死亡率が高いという結果でした(AHR 1.45、95% CI 1.22-1.72、P < .001)。
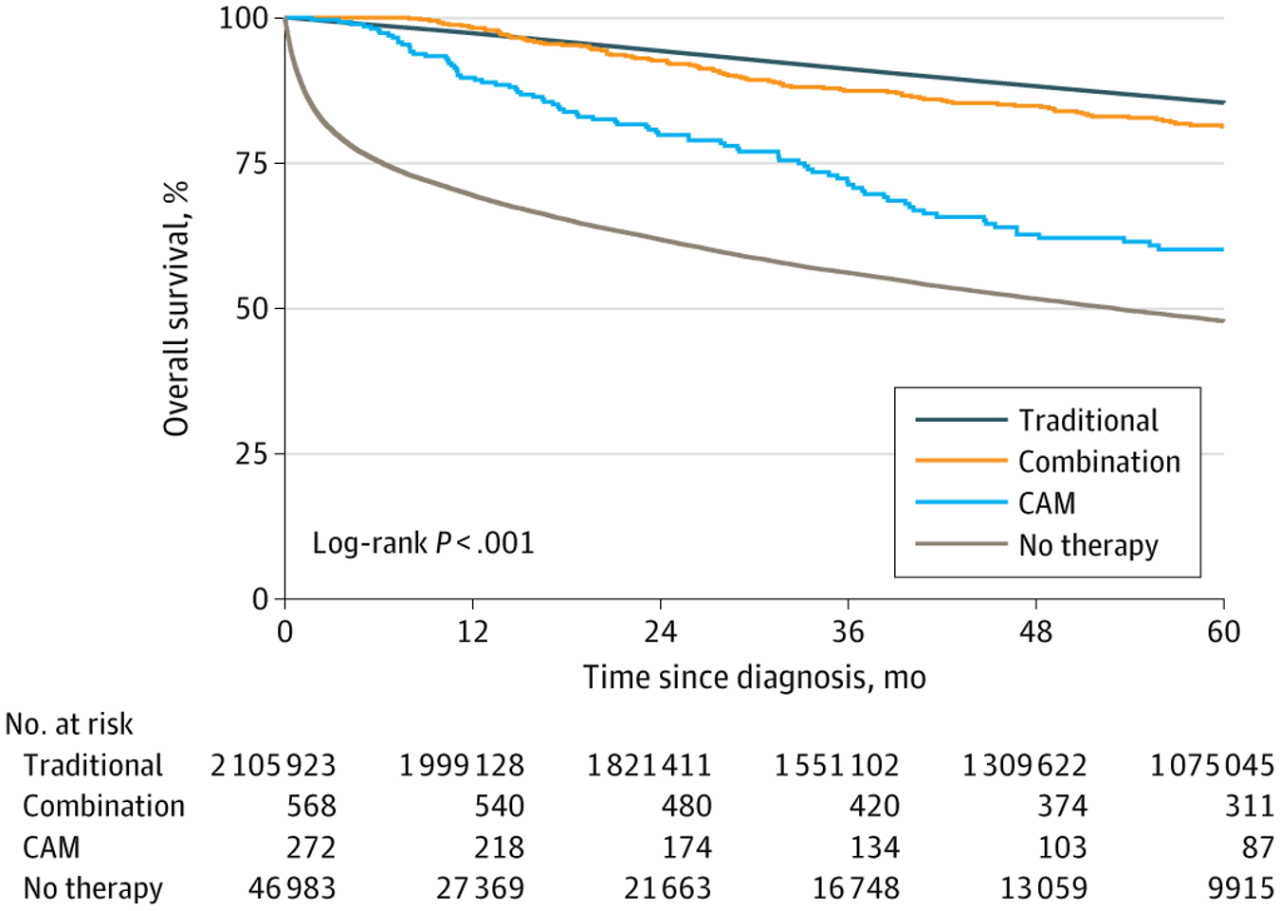
上のグラフはカプランメイヤー法によるもので、X軸で右に行くほど、時間が経過していることになります。12moと書いてあればそれは12か月経過した時点を指します。Y軸は生存率です。時間経過が0の時点では全員が生存していても、1年2年と経過するにつれ、亡くなる方が出て、生存されておられる方は減っていきます。つまり傾きが大きいグラフほど、生存率が低いという結果になります。
Traditional: 従来の標準治療
Combination: 標準治療と補完療法の併用
CAM: 代替療法のみ
No Therapy: 治療なし
今回の結果で、代替補完療法のみの患者さんが、治療なしよりも生存されていることには驚きました。そういう見方で見る方もおられるかもしれません。
ただ今回の研究は大規模ですが、それだけに様々な制限がかかっていると考えられます。
たとえば 今回の研究において代替療法とされた分類では、実は選択した多くの患者が見落とされている可能性があります。たとえば無治療とされても、実は補完療法を受けておられたり、標準治療のみとされていても、補完療法をこっそりされていたりです。その中には治療結果が大きく異なる患者もいるかもしれません。私の経験からしても、補完療法を併用されている方は0.1%程度では収まらないと思います。
ただそれを考えても、これだけの規模で比較すれば、小さな誤差は埋められると思います。
補完療法を受けられる方は、標準治療をきちんと完遂されない方が多く、そのため、治療成績が落ちる。
代替療法では、標準治療に成績では及ばない。
このことは今回の結果から明らかなのではないでしょうか?
ご予約専用ダイヤル
079-283-6103